Mocny i słaby kwas
Kwasy to substancje chemiczne, które przekazują jony wodoru lub protony po zmieszaniu w roztworach. Liczba protonów wydzielonych przez konkretny kwas faktycznie decyduje o sile kwasu - czy jest to silny kwas czy słaby kwas. Aby zrozumieć siłę kwasów, należy porównać ich skłonność do oddawania protonów do podobnej bazy (głównie wody). Siła jest oznaczana przez liczbę zwaną pKA.

Co to jest mocny kwas?
Uważa się, że kwas jest silny, jeśli dysocjuje całkowicie lub jonizuje w roztworze. Oznacza to, że jest w stanie podać największą liczbę jonów H + lub protonów po zmieszaniu w roztworze. Jony te są naładowanymi cząstkami. Ponieważ mocny kwas przekazuje większą liczbę jonów podczas rozkładu lub jonizowania, oznacza to, że silny kwas jest przewodnikiem elektryczności.
Kiedy kwas miesza się w H2O, proton (H.+ jon) przenosi się do H2Cząsteczka O do generowania H3O+ (Jon hydroksoniowy) i a - jon w oparciu o który kwas bierze udział.
W ogólnym scenariuszu

Takie reakcje chemiczne mogą być szanowane, ale w kilku przypadkach kwas daje H+ jon dość łatwo, a reakcja wygląda jak bycie jednokierunkowym. A kwas jest całkowicie rozłączony.
Na przykład, gdy chlorowodór rozpuszcza się w H2O do wytworzenia HCl, tak mało dzieje się tak, że możemy napisać:

W pewnym momencie zajdzie stuprocentowa wirtualna reakcja, w której chlorowodór będzie wykazywał reakcję z H3O+ (Jon hydroksoniowy) i Cl– jony. Silnym kwasem jest tutaj chlorowodór.
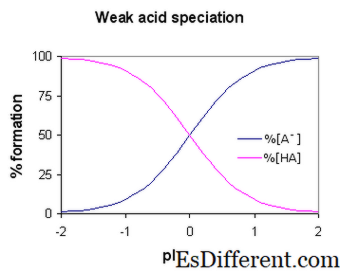
Co to jest słaby kwas?
Uważa się, że kwas jest słaby, jeśli jonizuje częściowo lub niecałkowicie, oddając tylko niektóre z jego atomów wodoru do roztworu. W związku z tym jest mniej zdolny w porównaniu z mocnym kwasem podczas wydawania protonów. Słabe kwasy mają wyższy pKa niż mocne kwasy.
Kwas etanowy jest dobrym przykładem słabego kwasu. Pokazuje reakcję z H2O do produkcji H3O+ (Jony hydroksoniowe) i CH3COOH (jony etanoanowe), ale reakcja odwrotna wykazuje większy sukces niż przedni. Cząsteczki reagują dość łatwo, aby złagodzić kwas i H2O.

W dowolnym momencie, tylko około jeden procent CH3Cząsteczki kwasu COOH wykazują przemianę w jony. Cokolwiek pozostało, to proste cząsteczki kwasu octowego (systematycznie zwane kwasem etanowym).
Różnica między mocnym kwasem i słabym kwasem
Mocny kwas
Silny kwas to kwas całkowicie jonizujący w roztworze wodnym. Silny kwas zawsze straci proton (A H +) po rozpuszczeniu w H2O. Innymi słowy, silny kwas jest zawsze na palcach i dość skuteczny w wydzielaniu protonów.
Słaby kwas
Słaby kwas to taki, który częściowo jonizuje w roztworze. Daje tylko kilka atomów wodoru w roztworze. Dlatego jest mniej zdolny niż silny kwas.
Mocny kwas
Silne kwasy zawsze będą wykazywać silne przewodnictwo. Silne kwasy zwykle przechodzą więcej prądu w porównaniu do słabych kwasów dla tego samego napięcia i stężenia.
Słaby kwas
Słabe kwasy mają niską przewodność. Są to słabe przewodniki i wykazują niską wartość prądu
Mocny kwas
Szybkość reakcji jest większa w silnych kwasach
Słaby kwas
Szybkość reakcji jest wolniejsza w słabych kwasach
Mocny kwas
Kwas chlorowodorowy (HCl), kwas azotowy (HNO3), Kwas nadchlorowy (HClO4), Kwas siarkowy (H.2WIĘC4), Kwas jodowodorowy (HI), kwas bromowodorowy (HBr), kwas chlorowy (HClO3).
Słaby kwas
Kwas siarkowy (H.2WIĘC3), Kwas octowy (CH3COOH), kwas fosforowy (H.3PO4), Kwas benzoesowy (C.6H5COOH), kwas fluorowodorowy (HF), kwas mrówkowy (HCOOH), kwas azotowy (HNO2).
Mocny kwas
W silnym kwasie pH jest niższe niż ogólnie 3. Mocne kwasy mają bardzo wysokie stężenie jonów H + (kwas o pH 3 ma 0,001 moli na litr jonów wodorowych).
Słaby kwas
Słaby kwas ma pH w zakresie 3-7.
Mocny kwas
W silnym kwasie wartość pKa jest dość niska.
Słaby kwas
W słabym kwasie wartość pKa jest dość wysoka.
Mocny kwas
HCl (g) + H2O (1) ≈ H3O+(aq) + Cl−(aq)
Słaby kwas
CH3COOH (l) + H20 (l) x H3O+(aq) + CH3GRUCHAĆ−(aq)
Podsumowanie silnych kwasów Vs. Słaby kwas
Punkty różnicowe między mocnymi i słabymi kwasami zostały podsumowane poniżej: Tabela porównawcza





